基础医学院医学遗传学系刘奇迹教授团队研究方向为遗传病致病基因鉴定及利用光遗传学手段进行干预治疗策略探索。近日,刘奇迹教授团队骨干李曦副教授在此领域取得原创性突破,实现了非病毒转染/非侵入式光调控对神经干细胞的动员和功能重塑,相关研究结果以“Nongenetic optical modulation of neural stem cell proliferation and neuronal/glial differentiation”为题发表在Biomaterials(2018年影响因子10.223)上。威尼斯欢乐娱人v3676为独立完成单位,文章第一作者为威尼斯欢乐娱人v3676基础医学院医学遗传学系2017级硕士研究生王梅天和已毕业的2012级硕士研究生许志亮,李曦副教授为该文章的通讯作者。
光生物医学是人类对于光线的创造性应用。如何在生物体内实现原位、非侵入式的光操控是光医学研究领域的核心科学问题。光遗传学从2006年提出到现在,极大地推进了神经调控领域的发展。然而,现有光遗传学技术普遍依赖病毒载体转染,需要将光敏蛋白的外源基因转染到成熟神经细胞,无法真正实现临床应用。因此,在哺乳动物神经系统中发现光敏响应体系,阐明其光感受/光转导通路,实现非病毒转染/非侵入式神经光调控,是该领域亟待解决的关键问题。
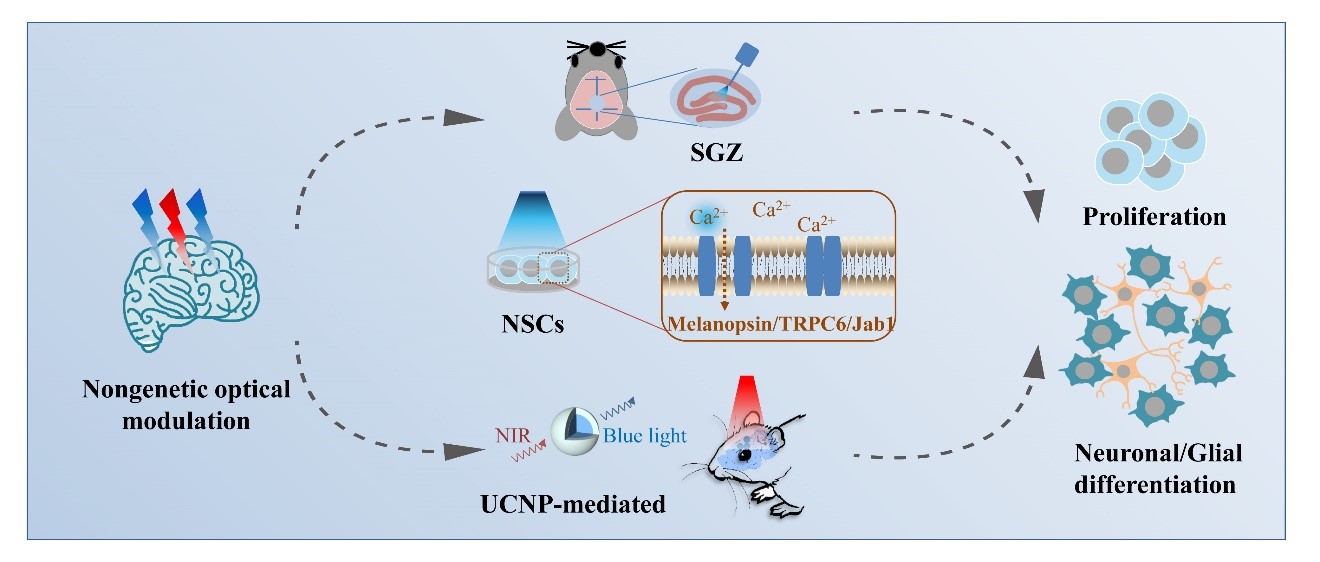
研究团队通过大量实验研究,发现小鼠神经干细胞自身表达多种光敏蛋白,细胞及分子遗传系列实验证明:无需病毒载体转染外源基因,通过微弱蓝光(455nm,300 µw/cm2)照射便可利用细胞内Melanopsin-TRPC6-Jab1分子信号通路,显著提升神经干细胞增殖分化行为。基于此体外实验结果,研究团队设计和开发了蓝光光纤植入定位照射技术,发现成年小鼠深部脑区的内源性神经干细胞同样表达此光感受/光信号转导通路,低剂量照射便可有效动员海马齿状回颗粒下区的内源性神经干细胞,实现功能重塑。研究团队进一步结合近红外光穿透组织性强、生物损伤小、适合非侵入式深部脑刺激的特点,在威尼斯欢乐娱人v3676晶体材料国家重点实验室刘铎教授的共同指导下,通过在小鼠深部脑区海马齿状回颗粒下区注射稀土掺杂上转换纳米颗粒,于脑外侧进行近红外光(980nm)照射,通过非线性效应在大脑深处诱导产生所需蓝光。研究结果显示该技术可以成功诱导静息态神经干细胞进行分化,实现了非侵入式内源性神经干细胞的体内原位动员。
该研究加深了人们对于神经干细胞光响应特征的理解,表明非病毒转染/非侵入式光调控可以实现对神经干细胞的动员,重塑神经功能,对于人们广泛关注的神经损伤及精神抑郁疾病的有效干预治疗具有重要的应用价值。课题在进展期间得到了基础医学院医学遗传学系龚瑶琴教授的大力支持。研究中激光共聚焦显微镜数据工作得到高等医学研究院医学基础研究平台的大力支持。
文章链接:https://www.sciencedirect.com/science/article/pii/S0142961219306386